六酸化四リン(ろくさんかよんリン、Tetraphosphorus hexoxide)は、分子式P4O6で表される化合物。三酸化リン (Phosphorus trioxide) や三酸化二リンとも呼ばれる。無色の固体であり、アダマンタンに関連する構造を持つ。形式上は亜リン酸(H3PO3)の無水物であるが、酸の脱水により得ることはできない。白色でワックス状であり、ニンニクの臭いのする結晶および非常に有毒な固体である。
調製
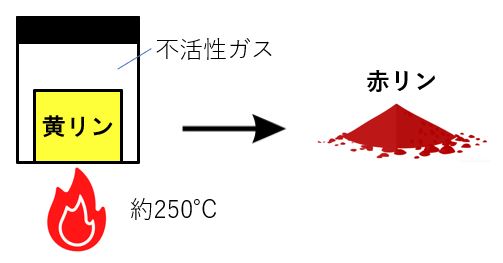
空気がわずかに供給されている状態でリンを低温で燃焼させることにより得られる。
- P4 3 O2 → P4O6
副生成物には赤リン亜酸化物が含まれる。
化学的性質
水と反応して亜リン酸を形成する。つまり、六酸化四リンは亜リン酸の無水物である。
- P4O6 6 H2O → 4 H3PO3
塩化水素と反応して亜リン酸と三塩化リンを形成する。
- P4O6 6 HCl → 2 H3PO3 2 PCl3
塩素または臭素と反応してそれぞれ対応するハロゲン化リンを形成し、密閉された管内で要素と反応し四ヨウ化二リンを形成する。
195Kでオゾンと反応し、不安定な化合物P4O18を生成する。
P4O18は238K以上の溶液中で分解し、O2ガスを放出する。乾燥したP4O18の分解は爆発的である。
不均化反応では、P4O6を密閉された管内で710Kで加熱すると、P(III)とP(V)が混合したP4O8に変換される。副生成物として赤リンが生成される。
配位子として
P4O6は、亜リン酸エステルに相当する遷移金属の配位子である。図の錯体はP4O6·Fe(CO)4である。BH3を用いると、二量体付加体が生成される。
出典